문익호의 화분
2022년 2회 수질환경기사 기출문제 : 1)수질오염개론 본문
1과목 : 수질오염개론
1. 하수가 유입된 하천의 자정작용을 하천 유하거리에 따라 분해지대, 활발한 분해지대, 회복지대, 정수지대의 4단계로 분류하여 나타내는 경우, 회복지대의 특성으로 틀린 것은?
① 세균수가 감소한다.
② 발생된 암모니아성 질소가 질산화된다.
③ 용존산소의 농도가 포화될 정도로 증가한다.
④ 규조류가 사라지고 윤충류, 갑각류도 감소한다.
답: ④
하천의 자정작용 4지대 (Whipple의 4단계)
1) 분해지대 : 오염된 물의 물리적, 화학적 성질이 나빠지며 오염에 약한 고등생물은 오염에 강한 미생물로 대체된다. 호기성 미생물의 활동에 의해 BOD(유기물질)가 감소한다.
2) 활발한 분해지대 : 용존산소가 없어 부패상태에 도달해 H2S에 의한 냄새 등 악취가 발생한다.
3) 회복지대 : 분해지대와 반대현상이 일어나 용존산소의 증가에 따라 물이 점차 깨끗해진다. 질산화 반응으로 아질산염(NO2), 질산염(NO3)의 농도가 증가하며 세균의 수는 감소하고 원생동물이 증가한다.
4) 정수지대 : 오염되지 않은 자연수처럼 보이며, 많은 물고기가 다시 번식하기 시작한다
2. 강우의 pH에 관한 설명으로 틀린 것은?
① 보통 대기중의 이산화탄소와 평형상태에 있는 물은 약 pH 5.7의 산성을 띠고 있다.
② 산성강우의 주요원인 물질로 황산화물, 질소산화물 및 염소산화물을 들 수 있다.
③ 산성강우현상은 대기오염이 혹심한 지역에 국한되어 나타난다.
④ 강우는 부유재(fly ash)로 인하여 때때로 알칼리성을 띨 수 있다.
답: ③
산성비는 넓은 지역으로 발생해 광범위한 피해를 입힌다.
빗물의 산도는 pH5.6정도가 이상적인 중성값
부유재 : 연료가 연소될 때 발생하는 배연 가스에 섞여 있는 미세한 재의 입자.
3. 호소의 부영양화에 대한 일반적 영향으로 틀린 것은?
① 부영양화가 진행된 수원을 농업용수로 사용하면 영양염류의 공급으로 농산물 수확량이 지속적으로 증가한다.
② 조류나 미생물에 의해 생성된 용해성 유기물질이 불쾌한 맛과 냄새를 유발한다.
③ 부영양화 평가모델은 인(P)부하모델인 Vollenweider 모델 등이 대표적이다.
④ 심수층의 용존산소량이 감소한다.
답: ①
부영양화 : 호수, 연안 해역, 하천 등의 정체된 수역에 오염된 유기물질(질소나 인)이 과도하게 유입돼 발생하는 수질의 악화현상
부영양화는 과다한 질소로 농작물의 성장 장애를 발생시킴
4. 수질오염물질 중 중금속에 관한 설명으로 틀린 것은?
① 카드뮴 : 인체 내에서 투과성이 높고 이동성이 있는 독성 메틸 유도체로 전환된다.
② 비소 : 인산염 광물에 존재해서 인 화합물 형태로 환경 중에 유입된다.
③ 납 : 급성독성은 신장, 생식계통, 간 그리고 뇌와 중추신경계에 심각한 장애를 유발한다.
④ 수은 : 수은 중독은 BAL, Ca2EDTA로 치료할 수 있다.
답: ①
카드뮴 : 투과성이 낮아 체내에 쌓이고 이로 인해 아연이 신경계에서 제 역할을 할 수 없게 되어 이타이이타이병을 일으킨다.
5. 광합성에 대한 설명으로 틀린 것은?
① 호기성광합성(녹색식물의 광합성)은 진조류와 청녹조류를 위시하여 고등식물에서 발견된다.
② 녹색식물의 광합성은 탄산가스와 물로부터 산소와 포도당(또는 포도당 유도산물)을 생성하는 것이 특징이다.
③ 세균활동에 의한 광합성은 탄산가스의 산화를 위하여 물 이외의 화합물질이 수소원자를 공여, 유리산소를 형성한다.
④ 녹색식물의 광합성 시 광은 에너지를 그리고 물은 환원반응에 수소를 공급해 준다.
답: ③
세균활동에 의한 광합성은 탄산가스의 환원을 위하여 물 이외의 화합물질이 수소원자를 공여, 유리산소를 형성한다.
6. 물의 특성에 대한 설명으로 옳지 않은 것은?
① 기화열이 크기 때문에 생물의 효과적인 체온 조절이 가능하다.
② 비열이 크기 때문에 수온의 급격한 변화를 방지해 줌으로써 생물활동이 가능한 기온을 유지한다.
③ 융해열이 작기 때문에 생물체의 결빙이 쉽게 일어나지 않는다.
④ 빙점과 비점사이가 100℃나 되므로 넓은 범위에서 액체 상태를 유지할 수 있다.
답: ③
물은 융해열이 크다. 융해열이 크기 때문에 생물체의 결빙이 쉽게 일어나지 않는다.
융해열 : 고체에서 액체로 변화하기 위해 필요한 에너지
7. 생물농축에 대한 설명으로 가장 거리가 먼 것은?
① 수생생물체내의 각종 중금속 농도는 환경수중의 농도보다는 높은 경우가 많다.
② 생물체중의 농도와 환경수중의 농도비를 농축비 또는 농축계수라고 한다.
③ 수생생물의 종류에 따라서 중금속의 농축비가 다른 경우가 많다.
④ 농축비는 먹이사슬 과정에서 높은 단계의 소비자에 상당하는 생물일수록 낮게 된다.
답: ④
생물농축 : 먹이사슬을 통해 독성물질이 농축되는 것
농축비는 먹이사슬 과정에서 높은 단계에 있을수록 높다.
8. 벤젠, 톨루엔, 에틸벤젠, 자일렌이 같은 몰수로 혼합된 용액이 라울트 법칙을 따른다고 가정하면 혼합액의 총 증기압(25℃기준, atm)은? (단, 벤젠, 톨루엔, 에틸벤젠,, 자일렌의 25℃에서 순수액체의 증기압은 각각 0.126. 0.038, 0.0126, 0.01177 atm이며, 기타 조건은 고려하지 않음)
① 0.047
② 0.057
③ 0.067
④ 0.077
답: ①
라울 법칙(Raoult's law) : 비휘발성, 비전해질인 용질이 녹아 있는 용액의 증기압 내림은 용질의 몰분율에 비례하며 또한 비휘발성 용액 속 용매의 증기압은 용매의 몰분율에 비례한다는 법칙

총 증기압은 각각의 증기압을 합한 것.
각각의 증기압은 순수액체 증기압 × 몰분율 이 되므로
벤젠 부분 증기압=0.126 X 0.25 = 0.0315
톨루엔 부분 증기압=0.038 X 0.25 = 9.5 X 10^-3
에틸벤젠 부분 증기압=0.0126 X 0.25= 3.15 X 10^-3
자일렌 부분 증기압=0.01177 X 0.25= 2.9425 X 10^-3
총 증기압=벤젠 부분 증기압 + 톨루엔 부분 증기압 + 에틸벤젠 부분 증기압 + 자일렌 부분 증기압 = 0.0.470925 = 0.047
9. BOD5가 270mg/L이고, COD가 450mg/L인 경우, 탈산소계수(K1)의 값이 0.1/day일 때, 생물학적으로 분해 불가능한 COD(mg/L)는? (단, BDCOD = BODu, 상용대수 기준)
① 약 55
② 약 65
③ 약 75
④ 약 85
답: ①
BDBOD : 생물학적으로 분해가능한 BOD (BODu)
NBDBOD : 생물학적으로 분해불가능한 BOD
COD = BDBOD + NBDBODBOD와 COD간의 관계식을 이용해 BDCOD 즉, BODu를 COD에서 빼주는 방식으로 구한다.BOD5를 이용해 소비 BOD공식으로 구하는 것이 요령.소비 BOD = Lo(1-10^(-k1*t))
※ 문제의 조건에서 상용대수이면 10을 적용하고 자연대수이면 e를 적용 ※
270 mg/L = Lo(1-10^(-0.1*5))
Lo = 394.87 (약 395)NBDBOD = COD - BDBOD = 450 mg/L - 395 mg/L = 55 mg/L
10. 다음은 수질조사에서 얻은 결과인데, Ca2+ 결과치의 분실로 인하여 기재가 되지 않았다. 주어진 자료로부터 Ca2+ 농도(mg/L)는?

① 20
② 40
③ 60
④ 80
답: ③
양이온과 음이온 각각의 몰수*당량 합이 서로 같아야 함.
양이온
(46/23)*1eq + (X/40)*2eq + (36/24)*2eq = 2+2(X/40)+3
음이온
(71/35)*1eq + (122/61)*1eq +(192/98)*2eq = 2+2+4 = 8
2+2(X/40)+3 = 8이 되어야 하므로
X= 60
11. 부영양화가 진행된 호소에 대한 수면관리 대책으로 틀린 것은?
① 수증폭기한다.
② 퇴적층을 준설한다.
③ 수생식물을 이용한다.
④ 살조제는 황산알루미늄을 주로 많이 쓴다.
답: ④
살조제 : 조류를 죽이는 성분을 지닌 물질 (황산구리, 황산동, 과산화수소, 염소, 오존)
12. 생물학적 질화 중 아질산화에 관한 설명으로 틀린 것은?
① Nitrobacter에 의해 수행된다.
② 수율은 0.04~0.13mg VSS/mg NH4+ -N정도이다.
③ 관련 미생물은 독립영양성 세균이다.
④ 산소가 필요하다.
답: ①
Nitrosomonas : 아질산화 관여 미생물
Nitrobactor : 질산화 관여 미생물
13. 0.01M-KBr과 0.02M-ZnSO4 용액의 이온강도는? (단, 완전 해리 기준)
① 0.08
② 0.09
③ 0.12
④ 0.14
답: ②
용액의 이온강도
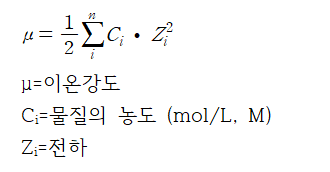
따라서
1/2{(0.01*1^2+0.01*1^2)+(0.02*2^2+0.02*2^2)} = 0.09
14. 바닷물에 0.054M의 MgCl2가 포함되어 있을 때 바닷물 250mL에 포함되어 있는 MgCl2의 양(g)은? (단, 원자량 Mg = 24.3, Cl = 35.5)
① 약 0.8
② 약 1.3
③ 약 2.6
④ 약 3.9
답: ②
바닷물에 MgCl2가 0.054M(mol/L)이 포함되어 있으므로 바닷물 1L 당 0.054mol의 MgCl2가 포함되어 있다는 것과 같다.
250ml는 1L의 1/4에 해당하므로 250mL에는 0.0135mol의 MgCl2가 포함되어 있다.
몰농도 = 질량 / 분자량
0.0135 = X / 95.3
X = 1.28655 (약 1.3)
15. 반응속도에 관한 설명으로 알맞지 않은 것은?
① 영차반응 : 반응물의 농도에 독립적인 속도로 진행하는 반응이다.
② 일차반응 : 반응속도가 시간에 따른 반응물의 농도변화 정도에 반비례하여 진행하는 반응이다.
③ 이차반응 : 반응속도가 한가지 반응물 농도의 제곱에 비례하여 진행하는 반응이다.
④ 실험치에 따라 특정 반응속도의 차수를 구하기 위하여는 시간에 따른 농도변화를 그래프로 그리고 직선으로부터의 편차를 구하여 평가한다.
답: ②
일차반응은 반응속도가 시간에 따른 반응물의 농도변화 정도에 비례하여 진행
16. 방사성 물질인 스트론튬(Sr90)의 반감기가 29년이라면 주어진 양의 스트론튬(Sr90)이 99% 감소하는데 걸리는 시간(년)은?
① 143
② 193
③ 233
④ 273
답: ②
방사성 붕괴 속도는 1차 반응에 해당.
C=Co*e^-kt
0.5=e^-29k에서 k=0.0239
스트론튬이 99% 감소할 때
0.01=e^-0.0239*t
t=192.68 (약 193년)
17. 수질모델링을 위한 절차에 해당하는 항목으로 가장 거리가 먼 것은?
① 변수 추정
② 수질예측 및 평가
③ 보정
④ 감응도 분석
답: ①
수질모델링 절차
1. 모델의 설계 및 자료수집
2. 모델링의 선정 및 예비적용
3. 보정(calibrataon)
4. 검증(verification)
5. 감응도 분석
6. 수질예측 및 평가
18. 다음과 같은 수질을 가진 농업용수의 SAR값은? (단, Na+ = 460mg/L, PO43- = 1500mg/L, Cl- = 108mg/L, Ca2+ = 600mg/L, Mg2+ = 240mg/L, NH3-N = 380mg/L, 원자량 = Na : 23, P : 31, Cl : 35.5, Ca : 40, Mg : 24)
① 2
② 4
③ 6
④ 8
답: ②
SAR(Sodium Adsorption Ratio) : 농업용수의 수질특성을 의미하는 것으로 Mg2+와 Ca2+농도에 대한 Na+농도의 비로 나타낸다.
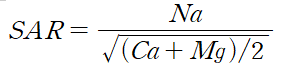
(여기서 Na+, Ca2+, Mg2+ 는 각각 해당 이온성분의 mEq/L의 단위로 입력)
mEq=mmol×원자가
mEq는 전해질의 농도를 나타내기 위해 만들어진 단위. 전해질의 화학적 결합력을 비교하기 위한 단위.
전해질은 질량(mmol)로 결합하는 것이 아니라 전하량으로 결합하기 때문에 Eq로 표시하며, 1/1000을 의미하는 m이 앞에 붙음.
Na+ 1mmol/L = 1mEq/L
Ca2+ 1mmol/L = 2mEq/L
다시 돌아와서 이온 농도를 mg/L → mEq/L로 변환
Na+ : 460mg/L × 1mmol/23mg = 20mmol/L = 20mEq
Ca2+ : 600mg/L × 1mmol/40mg × 2 = 30mEq
Mg2+ : 240mg/L × 1mmol/24mg × 2 = 20mEq
SAR = 20/{(30+20)/2}^0.5 = 4
19. 다음의 기체 법칙 중 옳은 것은?
① Boyle의 법칙 : 일정한 압력에서 기체의 부피는 절대온도에 정비례한다.
② Henry의 법칙 : 기체와 관련된 화학반응에서는 반응하는 기체와 생성되는 기체의 부피 사이에 정수관계가 있다.
③ Graham의 법칙 : 기체의 확산속도(조그마한 구멍을 통한 기체의 탈출)는 기체 분자량의 제곱근에 반비례한다.
④ Gay-Lussac의 결합 부피 법칙 : 혼합 기체내의 각 기체의 부분압력은 혼합물 속의 기체의 양에 비례한다.
답: ③
보일의 법칙 : 일정 온도에서 일정 질량의 기체가 가지는 압력과 부피의 곱은 일정하다.
헨리의 법칙 : 난용성기체에만 적용되며, 일정한 온도에서 용매에 녹는 기체의 질량은 압력에 비례한다.
게이-루삭의 법칙 : 화학반응에서의 기체의 부피는 간단한 정수비를 나타낸다.
20. 시료의 BOD5가 200mg/L이고 탈산소계수값이 0.15day-1일 때 최종 BOD(mg/L)는?
① 약 213
② 약 223
③ 약 233
④ 약 243
답: ④
BODt = BODu(1-10^(-k1*t))
※ 문제에 조건이 적혀있지 않으므로 상용대수 적용 ※
BODu = 200/(1-10^-0.15*5) = 243.26 (약 243)
'자격증 > 수질환경기사' 카테고리의 다른 글
| 2022년 2회 수질환경기사 기출문제 : 3)수질오염방지기술 (0) | 2022.08.07 |
|---|---|
| 2022년 2회 수질환경기사 기출문제 : 2)상하수도계획 (0) | 2022.08.06 |


